C'est une réaction :
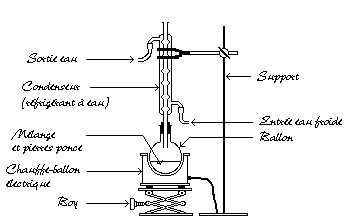
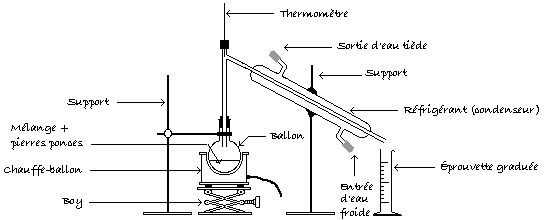
Quel montage est le plus adpté ?
-
Pourquoi chauffe-t-on le mélange réactionnel ?
- Pour augmenter le rendement de l'estérification.
- Pour augmenter la vitesse de réaction
- Pour atteindre tau = 100%
- Pour vaporiser l'eau produite, qui est génante
- Pour éviter des réactions parasites génantes
Pourquoi utilise-t-on le catalyseur H2SO4 ?
- Pour éviter des réactions parasites génantes
- Pour augmenter le rendement de l'estérification
- Pour augmenter la vitesse de réaction
- Pour atteindre tau = 100%
- Pour neutraliser les ions HO- produits
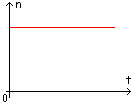
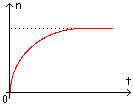
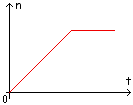
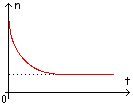
Soit n la quantité de méthanol dans le ballon. Comment évolue-t-elle au cours de l'estérification ?
-
Le taux d'avancement final vaut 67%. Calculer la quantité d'ester formé dans l'état final. (en mol )
Le système a atteint un état d'équilibre et Qr = K. Comment évolue le système si on ajoute de l'eau dans le ballon ?
- Déplacement dans le sens direct
- Equilibre inchangé
- Déplacement dans le sens inverse
Le système a atteint un état d'équilibre et Qr = K. Comment évolue le système si on ajoute de l'alcool dans le ballon ?
- Déplacement dans le sens direct
- Equilibre inchangé
- Déplacement dans le sens inverse